ACHIEVEMENTS
![]()
ACHIEVEMENTS研究成果
-

- ACHIEVEMENTS
- 「高親和性 ACE2 製剤はオミクロン株にも有効 新たな変異株や将来のパンデミックにも効果が期待される」
プレスリリース
2022.05.02
「高親和性 ACE2 製剤はオミクロン株にも有効 新たな変異株や将来のパンデミックにも効果が期待される」
京都府立医科大学大学院医学研究科 循環器内科学 星野温 講師 、大阪大学蛋白質研究所 高木淳一 教授、 高等共創研究院 岡本徹 教授 (微生物病研究所 、感染症総合教育研究拠点 兼任) 、微生物病研究所 ダロン・スタンドレー 教授 (感染症総合教育研究拠点 兼任 らの研究グループは現在開発中である高親和性 ACE2 製剤 がオミクロン株 B A.1, BA.2 に対しても有効であることを確認し、本研究成果は、2022年4月26 日に米国科学雑誌『Science Translational Medicine』誌に掲載されましたので、お知らせします。
現在問題となっているオミクロン株は既に報告されている通り、ワクチンや多くの中和抗体製剤に対して逃避性を示し、これらの有効性は大きく低下しています。 本研究では、ワクチン接種者やアルファ株、デルタ株感染者の血清では中和活性が約20 倍低下し 、カシリビマブとイムデビマブのカクテル抗体製剤も中和活性を喪失していることを確認しました。 一方、現在開発に取り組んでいる逃避変異が出現しにくい高親和性 ACE2 製剤 は オミクロン株に対しても有効で、さらに将来のパンデミックの原因となりうるコウモリなどに感染するコロナウイルスにも効果があることを確認しました。この高親和性 ACE2 製剤 は BA.2 系統を含むオミクロン株だけでなく、新たな変異株や将来のコロナウイルスパンデミックに対しても有効であることが期待されます。
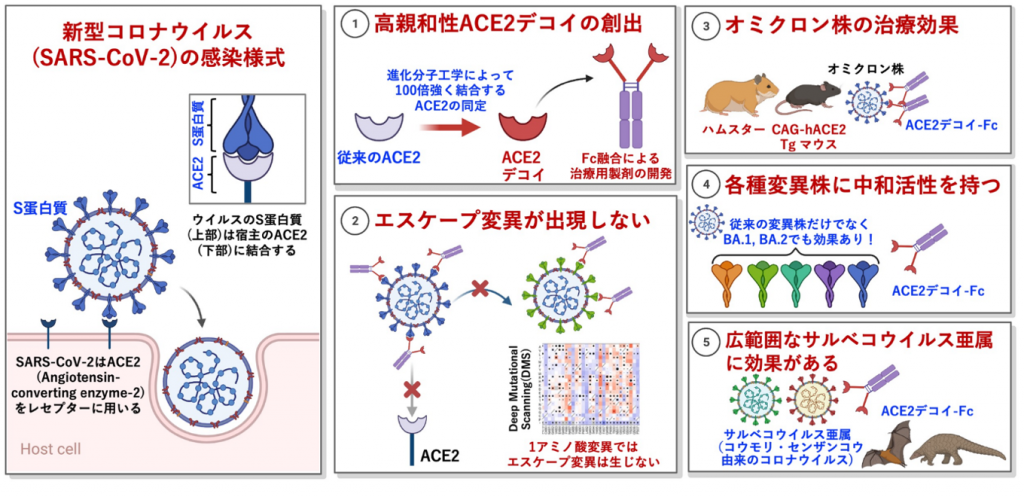
研究成果のポイント
⚫ ワクチン BNT162b2 2 回接種によるオミクロン株に対する中和活性は 、武漢株に対する中和活性と比較して約1 8分の 1 、アルファ株やデルタ株の感染者では1020分の1 低下していました。
⚫ オミクロン株は感染に重要な表面のスパイク タンパク質 に 3 0 個程度の変異がありますが、細胞表面の 感染受容体である ACE2 と直接結合する領域だけでなく、 N 末端領域における変異も逃避性に関与していました。
⚫ オミクロン株( BA.1 )に対する中和活性は 、現在日本で承認されている治療薬であるソトロビマブでは維持されていましたが 、カシリビマブ・イムデビマブのカクテル抗体製剤 では消失していました。 一方、我々が開発に取り組んでいる高親和性 ACE2 製剤 はオミクロン株BA.1 とその亜 型である B A.2 に対しても有効でした。
⚫ 高親和性 ACE2 製剤 は主要な変異株に対して有効性を確認しているだけでなく 、将来のパンデミックの原因となりうるコウモリやセンザンコウを宿主とする他のコロナウイルスに対しても有効性を示しました 。
⚫ スパイクタンパク質の全1アミノ酸変異を網羅したライブラリでの検討では、従来の中和抗体製剤と異なり、高親和性 ACE2 製剤 では中和活性が失われるアミノ酸変異は認められませんでした。そのため 、変異が高頻度に生じるウイルス治療薬において高親和性ACE2 製剤は抗体製剤より優れた治療薬モダリティであることが示唆されました。
本研究の背景
2021年11月に初めて確認されたオミクロン株は高い伝播力と免疫逃避性から一気に広がり、世界中でデルタ株からオミクロン株へ置き換わっています 。オミクロン株はスパイクタンパク質に約30 個もの変異が集積するこれまでにない進化が認められ、ワクチンやこれまでに開発された多くの中和抗体製剤が効果を失 いました。このようなウイルスの進化は今後も起こる可能性があるため、ウイルス変異の影響を受けない、すべての変異株に有効な治療薬が求められています。 我々が開発に取り組んでいる高親和性 ACE2 製剤は 新型コロナウイルスの感染受容体である ACE2 に基づいているため 、ウイルスが変異により本 製剤に結合しなくなった場合、細胞表面のACE2 とも結合できずに感染力を失うため実質的に逃避変異が生じないと考えられます。そこで高親和性 ACE2 製剤の幅広い有効性をオミクロン株や他のコロナウイルスに対して詳細に検討しました。
本研究の内容
<オミクロン株に対する中和活性>
まずワクチンのオミクロン株に対する有効性を 疑似ウイルス (注 1 により評価しました。BNT162b2 ワクチン 2 回目接種後 3 か月の血漿において武漢株 と比較するとオミクロン株に対しては中和活性が 17.7 倍低下していました。またアルファ株とデルタ株感染患者血漿では、武漢株やアルファ株、デルタ株と比較して、オミクロン株では 10 20 倍中和活性が低下していました。さらにスパイク タンパク質 の N 末端ドメイン NTD ;注 2 を入れ替えたキメラスパイクに対する中和活性の評価から、オミクロン株の免疫逃避性には受容体結合領域( RBD ;注 3 )の変異だけでなく NTDの変異も関与していることがわかりました。
<高親和性ACE2 製剤のオミクロン株に対する有効性>
現在日本では中和抗体製剤としてソトロビマブとカシリビマブ・イムデビマブのカクテル抗体製剤が承認されていますが、オミクロン株(BA.1)に対してソトロビマブは有効であるのに対してカクテル抗体製剤では中和活性が消失していました。一方、高親和性ACE2 製剤は亜型であるBA.2 も含めてオミクロン株に有効でした。さらにこの有効性は実際の生ウイルスを用いた実験でも確認され、更にハムスターでの感染モデルとヒトACE2 を発現したマウスでの感染モデル実験においてウイルス量の減少と死亡率の低下が確認されました(図1)。
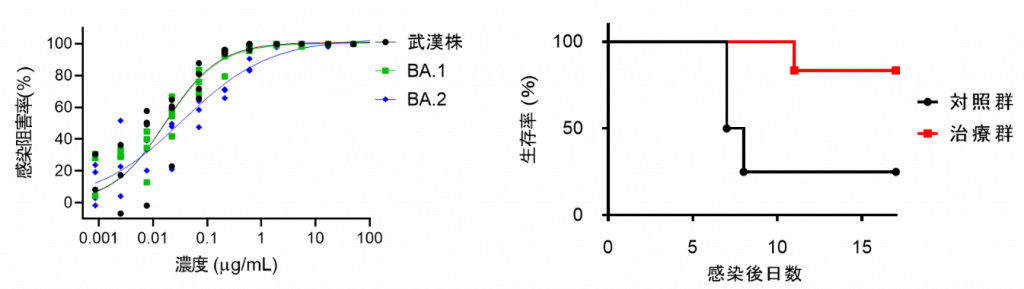
図1. 高親和性ACE2製剤のオミクロン株に対する中和活性(左図)、ならびにヒトACE2発現マウスにおける高親和性ACE2製剤のCOVID-19治療効果(右図)。BA.1とBA.2両方に対して中和活性が維持され、COVID-19マウスモデルで生存率の改善を認める。
<高親和性ACE2 製剤の幅広い有効性>
高親和性ACE2 製剤はオミクロン株だけでなく、これまでに発生したVOC(懸念される変異株)とVOI(注目すべき変異株)すべてに対して有効でした。さらにACE2 を感染受容体として利用するコロナウイルスは他にも存在し、多くはコウモリやセンザンコウを宿主としていますが、これらのサルベコウイルス亜属(注4)は将来のコロナウイルスパンデミックの原因となる心配があります。高親和性ACE2 製剤はこれらのコロナウイルスにも有効であることが確認されました。
<スパイクRBD 全1アミノ酸変異ライブラリによる検証>
高親和性ACE2 製剤の幅広い有効性を検証するために、既存の変異株だけでなく全ての1 アミノ酸変異スパイクタンパク質に対して検証を行いました。この評価系を用いるとカシリビマブでは図2 の矢頭で示すように逃避性変異を網羅的に同定することが可能になります。この手法を用いて検討したところ、高親和性ACE2 に対しては中和活性が消失するような逃避変異は認められず、ウイルスが変異により本製剤に結合しなくなった場合、細胞表面のACE2 とも結合できずに感染力を失うため実質的に逃避変異が生じない、という仮説が正しいことが確認できました。
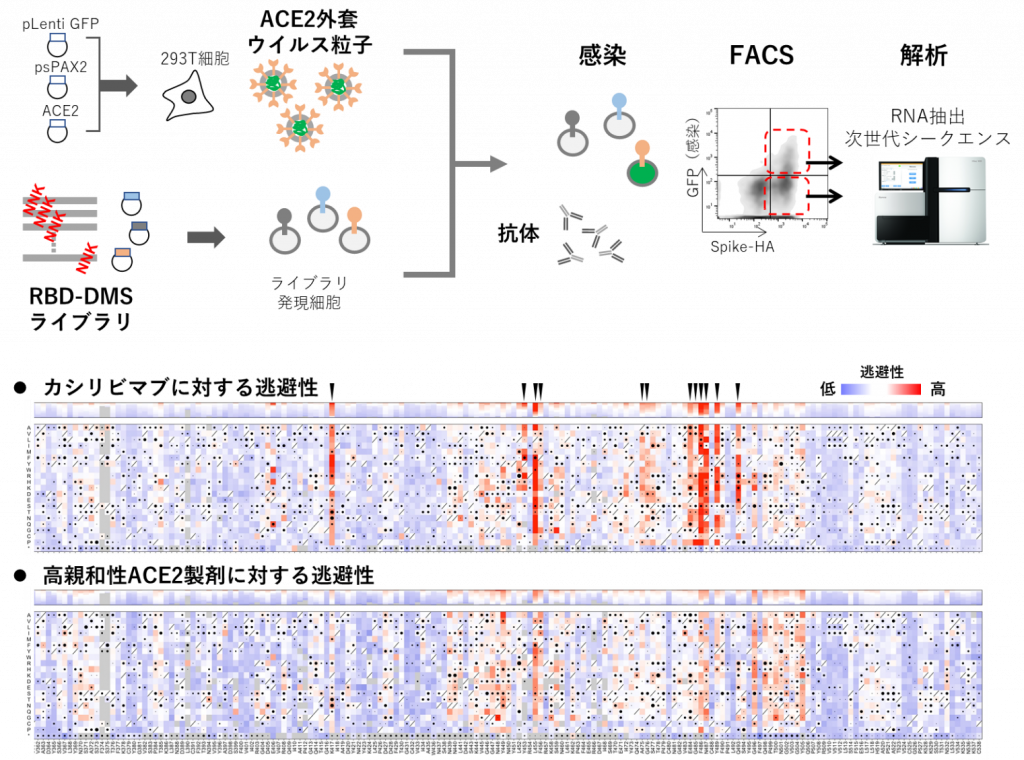
図2. スパイクRBDの全1アミノ酸変異に対する薬剤逃避性の網羅的評価の流れとその結果。カシリビマブでは、逃避性が高くなる箇所が見られるが、高親和性ACE2製剤では中和活性が消失するような逃避変異は認めらない。
まとめと今後の展開
高親和性ACE2製剤は抗体製剤と同等の中和活性を有し、さらに抗体製剤で問題となる逃避変異が出現しないため、変異株が頻繁に出現するウイルス感染症において非常に有用な治療モダリティになります。本研究結果から、新型コロナウイルスの変異株だけでなく、将来のコロナウイルスパンデミックに対しても有効な可能性があると考えられることから、これらに対する備蓄薬としての用途も期待されます。現在はサルの感染モデルで有効性と安全性の評価を行っています。
【用語解説】
(注1) 疑似ウイルス:レトロウイルスの粒子表面のエンベロープタンパク質を別のウイルス由来のものに置き換えたウイルスで、今回はエンベロープタンパク質の代わりに新型コロナウイルスのスパイク(S)タンパク質を外套させている。危険性の高い新型コロナウイルスの代わりに疑似ウイルスを用いる事で比較的安全に実験が行える。
(注2) N末端ドメイン:スパイクタンパク質のアミノ末端領域で機能はよくわかっていない。
(注3) 受容体結合領域:新型コロナウイルスのスパイクタンパク質が細胞の受容体であるACE2と結合する領域。
(注4) サルベコウイルス亜属:ウイルスの分類学上、コロナウイルス科-βコロナウイルス属の下位で新型コロナウイルスなどACE2受容体を利用して宿主細胞に侵入するウイルスが分類される亜属
掲載論文・雑誌
An engineered ACE2 decoy neutralizes the SARS-CoV-2 Omicron variant and confers protection against infection in vivo
「改変ACE2受容体は免疫逃避性を示すオミクロン株も中和する」
Nariko Ikemura*, Shunta Taminishi*, Tohru Inaba*, Takao Arimori*, Daisuke Motooka*, Kazutaka Katoh*, Yuhei Kirita, Yusuke Higuchi, Songling Li, Tatsuya Suzuki, Yumi Itoh, Yuki Ozaki, Shota Nakamura, Satoaki Matoba, Daron M Standley†, Toru Okamoto†, Junichi Takagi†, Atsushi Hoshino†
†責任著者:星野 温、高木 淳一、岡本 徹、ダロン・スタンドレー
Science Translational Medicine 4月26日オンライン掲載
DOI: 10.1126/scitranslmed.abn7737
オンライン掲載URL: http://www.science.org/doi/10.1126/scitranslmed.abn7737
なお本研究内容は論文掲載に先立ち、以下のとおりプレプリントリポジトリにて公開されました。
・2021年12月13日付 medRxiv投稿
タイトル:SARS-CoV-2 Omicron variant escapes neutralization by vaccinated and convalescent sera and therapeutic monoclonal antibodies
DOI: https://doi.org/10.1101/2021.12.13.21267761
・2021年12月22日付 bioRxiv投稿
タイトル:Engineered ACE2 counteracts vaccine-evading SARS-CoV-2 Omicron variant
DOI: https://doi.org/10.1101/2021.12.22.473804
特記事項
本研究は、日本医療研究開発機構(AMED) 新興・再興感染症に対する革新的医薬品等開発推進研究事業、創薬等ライフサイエンス研究支援基盤事業(BINDS)、そして先進医薬研究振興財団の研究支援を受けて実施されました。






